1
Автор статьи: Марина Дмитриевна
2017.10.01
12 354
Анализ крови
Анализ крови – главное и первое исследование, которое назначают врачи при поступлении пациента в больницу. Он полно, быстро и дешево выдает объем информации о состоянии больного. Однако такие анализы различны, один из вариантов – исследование на количество бластных телец. Что это, зачем они нужны и какой нормальный уровень в крови? Разберемся!
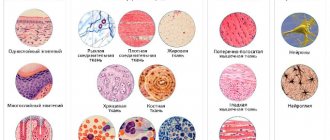
Определение клеток под микроскопом
Бластные клетки: их количество и состояние в здоровом организме
Когда у человека не диагностировано никакой болезни, нет стресса, каких либо инфекционных заболеваний или других факторов, имеет место следующее:
- в кровотоке бластные клетки полностью отсутствуют;
- в костном мозге их зафиксировано не более 5% от общего количества клеток.
Повторимся: в норме бластные клетки в анализе крови должны полностью отсутствовать; на бланке результата должно быть написано “0%”. Даже малое количество бластов в кровотоке – очень серьезный повод для обращения к врачу и проведения дополнительных исследований.
Что значат нормобласты в крови
Общий анализ крови регулярно используется медицинскими работниками с целью выявления скрытых заболеваний. Расшифровка полученных результатов осуществляется благодаря специальным таблицам с показателями рассчитанной нормы для каждого компонента биоматериала.
При наличии каких-либо патологий у пациента будет нарушено соотношение маркеров. Однако, если лейкоциты или эритроциты обязательно должны выявляться на диагностике, то бласты в крови зачастую будут свидетельствовать о нарушениях в работе иммунной системы.
Что представляют собой нормобласты?
Бластные клетки – это промежуточная форма эритроцитов (красных кровяных телец), отвечающих за насыщение тканей тела кислородом, а также выведение из организма углекислого газа.
Данные вещества формируются, как и все форменные элементы крови, в костном мозге. Иссиня-фиолетовые клетки на данном этапе развития активно обогащаются гемоглобином, который провоцирует уменьшение ядра.
Когда оно полностью растворится, нормобласты приобретут более миниатюрные размеры и преобразуются в ретикулоциты розоватого оттенка.
Бластные клетки в анализе крови под микроскопом
Они, в свою очередь, покидают свою обитель, поступая непосредственно в кровоток, где на протяжении 1–3 дней избавляются от ненужных органоидов (митохондрий, эндоплазматической сети). Ретикулоциты уже могут осуществлять перенос кислорода, однако их функциональность значительно повышается после полноценного превращения в эритроциты двояковогнутой формы.
Нередко специалисты при расшифровке показателей упоминают нормоциты или бластоциты. Необходимо запомнить, что эти термины являются медицинской интерпретацией нормобластов.
Если уровень содержания бластов в крови достаточно повышен, организм может быть поражен следующими заболеваниями:
- остеосаркома;
- патология Ди Гульермо;
- острый эритролейкоз;
- миелобластная анемия;
- рак костного мозга;
- глиобластома;
- множественные метастазы;
- лимфобластный лейкоз;
- талассемия;
- гепатома;
- экстрамедуллярное кроветворение;
- мегалобластическое малокровие;
- гипопластическая анемия;
- бронхогенная карцинома.
Иногда причиной появления нормобластов в анализе крови является гемолиз – болезнь, характеризующаяся патологическим разрушением эритроцитов с выделением в кровь гемоглобина.
Когда организм человека теряет важнейших переносчиков углекислого газа и кислорода, развивается гипоксия.
Для того чтобы избежать необратимых последствий, на помощь иммунной системе костный мозг посылает нормобласты, которые временно замещают своих более зрелых «собратьев».
Нередко количество нормоцитов диагностируется у женщин после обильных менструаций или тяжелых родов, которые повлекли за собой повреждение внутренних органов. Если пациент ранее перенес инфекционное заболевание, в результатах его общего анализа крови, скорее всего, тоже обнаружатся нормоциты.
Серьезная кровопотеря, вызванная тяжелым ранением, в норме будет характеризоваться появлением нормобластов, стабилизирующих функцию кроветворения
Как проводят забор крови?
Как правило, для процедуры ОАК требуется капиллярная кровь из безымянного пальца. После того как его подушечка будет продезинфицирована медицинским спиртом, производится безболезненный прокол с помощью автоматического скарификатора. Периодически сжимая палец у ногтевой пластины, лаборант набирает около 2–3 мл биоматериала с помощью стеклянного капилляра.
Когда пробы крови будут распределены по емкостям, ранку снова дезинфицируют и накладывают на нее стерильный ватный диск. Намного реже для лабораторного исследования берут венозную кровь из локтевого сосуда. В таком случае сначала накладывают на плечо жгут и обрабатывают место пункции, после чего иглу вакуумной системы или одноразового шприца вводят в вену.
Угол наклона иглы постепенно уменьшают, облегчая забор материала. Как только процедура завершится, к области прокола прижимают марлевый тампон, выводят иглу из сосуда и снимают жгут. Придерживать ватку нужно до тех пор, пока ранка не закупорится кровяным сгустком, иначе в области сгиба образуется болезненная подкожная гематома.
Подготовка к диагностике
Анализ крови на РФМК + расшифровка
Получив результаты общего анализа, лечащий врач никогда не будет оценивать лишь один его параметр, не обращая внимания на остальные.
Для того чтобы баланс количественного содержания всех форменных элементов крови помимо нормобластов не был искусственно нарушен, следует на протяжении нескольких дней перед диагностикой придерживаться некоторых правил подготовки.
За неделю до процедуры нужно сообщить специалисту перечень принимаемых препаратов, чтобы он мог оценить степень их воздействия на состав крови. Если некоторые медикаменты вызывают нежелательные изменения, их использование временно приостанавливается. За 3–4 дня из рациона изымаются вредные продукты и напитки, особенно фастфуд, алкоголь, маринады, жирная и жареная пища.
Также необходимо на 1–2 дня прекратить спортивные занятия, бег и плавание не являются исключением. Посещать медицинское учреждение следует натощак. Курить перед диагностикой запрещается. Если пациент спешно пришел в клинику, ему обязательно нужно отдышаться, прежде чем заходить в кабинет.
Не рекомендуется накануне забора крови злоупотреблять кондитерскими изделиями – превышение дневной дозировки сладостей влечет за собой ложный результат исследования
Всегда ли повышенный уровень – признак патологии?
Вовсе нет. Например, нормобласты в общем анализе крови у абсолютно здоровых младенцев до 3–4 месяцев – вполне допустимое явление, связанное с активным физиологическим формированием маленького организма.
У детей старшего возраста бластоциты должны наблюдаться лишь в области костного мозга, а не в крови.
Если забор биоматериала осуществляется у пациента с пернициозным (злокачественным) малокровием, тогда выявление нормоцитов считается предвестником скорой ремиссии.
При подобных обстоятельствах бластные клетки будут свидетельствовать о наличии функциональности защитных механизмов. Более того, люди иногда получают неутешительные результаты, которые перечеркивались показателями повторной диагностики. Поэтому не стоит переживать, увидев тревожные цифры на бланке, нужно спокойно посетить специалиста с целью их подтверждения или опровержения.
Источник: https://apkhleb.ru/krov/chto-znachat-normoblasty-krovi
Сдвиги в формуле при изменении состояния здоровья
Если в костном мозге содержится 1% бластов – это стандарт, указывающий на то, что всё с организмом хорошо. Результат от 5% до 10% – не норма, однако это ещё не показатель определенного гематологического заболевания.
Бласты в костном мозге в таком количестве могут быть либо в результате сильного стресса, либо как следствие острого инфекционного процесса.
Если бластные клетки в костном мозге обнаруживаются в количестве более 10%, это повод для врача поставить диагноз “лейкоз”.
Однако такой диагноз ставится по совокупности факторов:
- низкие эритроциты, тромбоциты и гемоглобин;
- высокие лейкоциты;
- наличие бластных клеток в кровотоке;
- наличие бластов в костном мозге в количестве более 10%.
Важно отметить то, что анализ на определение количества незрелых кровяных телец не делается самостоятельно; на него, как правило, направляет врач – терапевт или гематолог – при наличии веских оснований. Например, если больной на осмотре предъявляет жалобы, по которым можно было бы поставить диагноз “лейкемия”, доктор может направить такого пациента на анализ, где определят, превышена ли у него норма бластных клеток в крови.
Бластные клетки в анализе крови – что это за клетки, их норма в крови и о чем говорят отклонения
Анализ крови – главное и первое исследование, которое назначают врачи при поступлении пациента в больницу. Он полно, быстро и дешево выдает объем информации о состоянии больного. Однако такие анализы различны, один из вариантов исследование на количество бластных телец. Что это, зачем они нужны и какой нормальный уровень в крови? Разберемся!
Что такое бластные клетки?
Кровь – важнейшая жидкость в организме человека. Выполняет множество функций,: от питания до защиты органов от инфекций и бактерий. За каждую «задачу» отвечают клетки крови, например: эритроциты – красные кровяные тельца, доставляют кислород в уголки человеческого тела.
Предшественниками элементов крови являются бласты. Развиваются в спинном мозге и по мере необходимости превращаются в эритроциты, лейкоциты и так далее. Здоровые тельца готовы «преобразиться» во время острых кризисов в больших количествах, появляясь в крови в виде защитных или других клеток.
Что такое острый лейкоз?
Острый лейкоз следствие нарушения в работе кроветворения на сначальных стадиях. В нормальном состоянии бластные клетки превращаются в функциональные клетки крови и выполняют свою миссию. Каждое такое тельце сразу после «появления на свет» имеет свою линию развития. Например: для эритроцитов «производятся» один вид таких клеток, а для лейкоцитов другой и так далее.
https://www.youtube.com/watch?v=9L2fgTdUUSg
Когда кроветворная система дает сбой, и создание здоровых базовых клеток нарушается, тельца ведут себя по-другому.
Они не превращаются в «рабочие» клетки – только потребляют полезные вещества и размножаются. Со временем заменяют здоровые клетки и проникают в кости, разрушая их, не поставляя полезных веществ.
Резко снижается количество полезных клеток, падает гемоглобин, тромбоциты и лейкоциты.
Такая болезнь лимфобластная и миелобластная – в зависимости от того, какой тип клеток стал «виновником» заболевания. Подразделяются на другие, более мелкие категории, в зависимости от предназначения поврежденных бластных элементов.
Обозначаться могут, например: острый В-лимфобластный лейкоз, что подразумевает сбой в создании бластов на уровне «производства» таких элементов, как В-лимфоциты или острый монобластный лейкоз, который возник при проблемах в создании моноцитов. В зависимости от степени сложности и вида лейкоза прогнозы на излечение пациента разные.
Подготовка к анализу на наличие бластов в крови
Чтобы результат анализа не был искажен и его не пришлось пересдавать, рекомендуется соблюсти несколько простых правил:
- последний прием пищи должен быть за 8 часов до теста;
- за день до исследования не следует употреблять любые спиртные напитки;
- за 2 часа до анализа исключите воздействие никотина на организм;
- рекомендуется прекратить прием лекарств за 72 часа до анализа.
Если какой-то из пунктов выполнить не представляется возможным, нужно обязательно сказать об этом лаборанту, который будет брать у вас кровь.
Сообщите ему обо всех принятых лекарствах за 3 дня до анализа лекарствах. Если вы по состоянию здоровья не можете долго обходиться без еды, обязательно скажите лаборанту, что конкретно вы употребили в пищу. Эта информация поможет правильно скорректировать результаты анализа. Они всё равно, скорее всего, будут искаженными, однако врач в заключении сумеет правильно отразить информацию с учётом переданных вами сведений.
Как распознать лейкоз по анализу крови?
Врач-гематолог, доктор медицинских наук Сергей Семочкин про острый лимфобластный лейкоз
Врач-гематолог, профессор кафедры онкологии, гематологии и лучевой терапии РНИМУ им. Н. И. Пирогова Минздрава России, доктор медицинских наук Сергей Семочкин рассказал: можно ли распознать острый лимфобластный лейкоз (ОЛЛ) на ранней стадии и поставить диагноз по анализу крови; объяснил, как лечат ОЛЛ и кому показана трансплантация костного мозга (ТКМ).
Каковы ранние симптомы острого лимфобластного лейкоза? Можно ли их увидеть и распознать ОЛЛ?
В данном случае все достаточно просто, потому что слово «острый» означает, что заболевание внезапное и зачастую симптомы очень выразительные. Самый частый симптом – это лихорадка, т.е. повышение температуры тела.
Лихорадка может быть как субфебрильной, так и ярко выраженной, до 39 градусов. Появятся изменения, связанные с поражением костного мозга. Снижение гемоглобина приведет к слабости и быстрой утомляемости.
Могут увеличиться лимфатические узлы, появиться дискомфорт в брюшной полости за счет того, что увеличиваются размеры печени и селезенки. Могут быть проявления кровоточивости – даже во время чистки зубов.
У некоторых пациентов ОЛЛ может начаться с неврологических проявлений – головных болей, головокружения и прочих проблем. Симптоматика обширная, но в данном случае она является достаточно острой, внезапно возникшей.
Смотрите видео на нашем сайте.
Можно ли поставить диагноз по анализу крови? Что он покажет?
Как правило, в анализе крови есть ярко выраженные показатели: изменены ростки кроветворения, количество лейкоцитов выходит за пределы нормы – может упасть ниже нормальных значений, а может стать запредельно огромным. Мне встречались пациенты, у которых количество лейкоцитов при норме от 4 до 9 тысяч повышалось до 200 тысяч на мкл.
Тромбоциты тоже в ряде случаев очень сильно снижены, но главное – изменение количества лейкоцитов. Очень важным маркером является выход опухолевых клеток в кровь, когда в крови появляются незрелые ранние клетки, которые называют бластными.
Если в анализе крови выявили бластные клетки, то это, скорее всего, либо острый лейкоз, либо миелодиспластический синдром.
Как пациент попадает к гематологу?
Анализ крови с характерными изменениями – повод для немедленного вызова скорой помощи и госпитализации пациента в профильный стационар. При лечении детей и подростков у онкогематолога, как правило, есть один-два дня ни диагностику, лечение необходимо начинать, как можно раньше.
В диагностику входит повторный анализ крови, затем – верификация диагноза, для которой проводят биопсию костного мозга. У маленьких детей ее проводят под общей анестезией, у взрослых – под местной. С помощь небольшой иглы делаю прокол грудины или подвздошной кости. У детей пункцию грудины не делают.
Полученный образец костного мозга, который выглядит как обычная пробирка с кровью, отправят в лабораторию, где для подтверждения диагноза проведут целый спектр исследований. Главный критерий – увеличение количества бластных клеток. Только по внешнему виду и по количеству бластных клеток определить вариант лейкоза – невозможно.
Еще в 1913 году установили, что есть лимфоидный, а есть миелоидный вариант лейкоза. Для верификации применяются специальные лабораторные методы: иммунологические и химические. Существует специальный прибор – проточный цитометр, с помощью которого определяют маркеры, характеризующие данный тип клеток.
Для определения подвида острого лейкоза, применяют целый спектр генетических исследований, чтобы выйти на более целевую терапию у этих пациентов.
Каковы причины возникновения ОЛЛ? Существует мнение, что этот вид лейкоза очень сильно взаимосвязан с экологическими проблемами, передается по наследству и часто возникает у тех, кто уже переболел каким-то онкологическим заболеванием. Правда это или нет?
Истинную причину возникновения лейкоза у взрослых можно выявить только в 5% случаев, в 95% совершенно непонятно, что там к чему привело. У детей все несколько интересней.
Как возникает лейкоз? В генетическом материале клетки возникает некая первичная мутация, которая сама по себе далеко не всегда приводит к лейкозу.
В дальнейшем к этой мутации присоединяются другие, и когда болезнь все же возникает, в клетке накоплено уже много молекулярных событий, сочетание которых привело возникновению заболевания.
Пик острого лимфобластного лейкоза приходится на детей от двух до четырех лет, потом заболеваемость падает. Следующий пик приходится на 18-29 лет, потом снова спад. После 60 лет – опять небольшой рост.
У части детей раннего возраста прослеживается некая врожденная составляющая этой проблемы. Встречаются случаи ОЛЛ у плода или новорожденного, когда ребенок рождается уже с заболеванием, либо заболевает в течение первого года жизни. Исследования пуповинной крови показали, что у новорожденных встречаются лейкемические поломки, врожденные мутации, которые могут привести к возникновению лейкоза.
И мутацию эту вызывает наследственный фактор, сработавший во время внутриутробного развития. По разным данным, общее количество таких младенцев составляет от 1 до 5%. Дальше многое зависит от инфекционной обстановки, сложившейся вокруг ребенка. Многочисленные инфекции, перенесенные в детстве, способствуют формированию нормальной иммунной системы, которая нейтрализует наследственный фактор.
Если говорить про экологические проблемы, то с ними четкой связи не выявлено.
Влияет ли УФ-излучение, СВЧ, солнечные лучи, радиация?
В Хиросиме и Нагасаки повышенная заболеваемость держалась около 12 лет. После Чернобыля у многих пострадала щитовидная железа, но заболеваемость лейкозами не выросла. Все зависит от типа изотопов попавших в окружающую среду. В Фукусиме тоже этого не случилось, потому что концентрация радиоактивных веществ сильно разбавилась морской водой.
Вред ультрафиолета научно доказан только в отношении меланомы. Четкой связи с ОЛЛ нет. Своим бывшим пациентам мы не разрешаем посещать солярий и не рекомендуем загорать, потому что хотя связь и не доказана, совсем исключать этот фактор тоже нельзя.
Если говорить об СВЧ-излучении, домашние микроволновые печи абсолютно безопасны.
Как лечат ОЛЛ? Что ждет пациента?
Концепция лечения ОЛЛ, которая до сих поре лежит в основе протоколов лечения ОЛЛ, была разработана американским педиатром Дональдом Пинкелем еще в 1962 году. Она включает в себя четыре этапа: индукция ремиссии, консолидация, воздействие на центральную нервную систему и длительный этап поддерживающей терапии на протяжении двух-трех лет.
Во всем мире проводится лечение по клиническим протоколам, разработанным в результате кооперированных исследований. Согласно некоторым работам, строгое следование протоколам повышает выживаемость пациентов на 15-20% по сравнению с индивидуализированным лечением. В протоколе прописаны все действия: от первого дня до последнего.
В нем есть указания, как и в какой момент оценивать возникающие осложнение и что с ними делать. В России два центра, активно ведущих такие протоколы. Центр им. Дмитрия Рогачева, где Александр Исаакович Карачунский в течение многих лет, с начала 1990-х, ведет серию протоколов «Москва – Берлин».
Каждые пять лет дизайн протоколов пересматривают, чтобы улучшить лечение отдельных категорий пациентов. уже в течение многих лет с начала 90-х годов серию протоколов Москва-Берлин. Каждые пять лет меняется дизайн протоколов, направленных на улучшение лечения отдельных категорий пациентов.
Во взрослой практике – это НМИЦ гематологии, где ведут кооперированные исследования по острому лимфобластному лейкозу у взрослых.
В каких случаях показана трансплантация костного мозга (ткм)?
В отличие от острого миелоидного лейкоза, показаний к аллогенной (от донора) ТКМ меньше. Ее назначают пациентам, которые не достигли ремиссии в указанные протоколом сроки или имеют неблагоприятный цитогенетический вариант заболевания. В детской практике выздоравливают более 90% детей, и примерно 15-20% являются кандидатами для аллогенной ТКМ.
У взрослых процент пациентов нуждающихся в трансплантации несколько выше, за счет того, что генетических операций высокого риска становится намного больше и ответ на стандартное лечение хуже. Когда мы обсуждали хронический миелолейкоз, там фигурировала филадельфийская хромосома – транслокация (9;22). При ОЛЛ это абсолютно негативный фактор прогноза.
У детей такая мутация встречается меньше чем в 5% случаев, у людей старше 50-60 лет примерно половина В-линейных ОЛЛ будет с филадельфийской хромосомой. В отличие от хронического миелолейкоза, применение ингибиторов тирозинкиназы при остром лимфобластном лейкозе не столь успешно. Вот поэтому во взрослой практике ТКМ необходимо проводить примерно 30% пациентов.
Возрастной порог для аллогенной ТКМ – в районе 55 лет, это разумно.
Как часто случаются рецидивы с ОЛЛ?
Если мы говорим про взрослых людей, то рецидивы случаются почти в 40% случаев. Бывают ранние рецидивы, которые случаются прямо на терапии.
В таком случае необходимо менять лечение, делать его более интенсивным и тяжелым. В таких случаях, как правило, показана ТКМ. Поздний рецидив может случиться и через 20 лет.
К сожалению мы не можем убрать причину, которая вызывает это заболевание – оно может вернуться.
Можно ли планировать беременность после ОЛЛ?
Длительная химиотерапия нарушает фертильность, поэтому лучше провести криоконсервацию спермы/яйцеклетки, а еще лучше эмбриона – это более надежный способ. У мужчин, как правило, серьезно нарушается сперматогенез, но у женщин дело обстоит несколько лучше. Вероятность забеременеть и выносить здорового ребенка высока. Если прошло не менее пяти лет в ремиссии, никаких ограничений нет.
Может ли беременность быть провоцирующим фактором для рецидива?
Скорее, нет. Это не такое частое явление, как при некоторых других заболеваниях, где беременность действительно может стать провоцирующим фактором.
Передается ли ОЛЛ по наследству?
Лимфобластный лейкоз – редкое заболевание, поэтому вероятность того, что он случится у ребенка, рожденного от родителей после ОЛЛ, крайне мала.
Как будут лечить ОЛЛ в будущем?
Представляется, что в основе лечения онкологических заболеваний в будущем станет активация собственного иммунитета. Нам необходимо настроить иммунную систему таким образом, чтобы она распознавала и убирала раковые клетки.
Сейчас мы находимся на раннем этапе развития CAR-T-терапии, но через какое-то время технологии настолько усовершенствуются, что, скорее всего, она станет одним из основных методов терапии при целом ряде онкогематологических заболеваний.
Суть метода заключается в том, что у пациента собирают его собственные Т-лимфоциты и отправляют в специальную лабораторию. Эта лаборатория может быть в другом городе, стране – не важно. В лаборатории эти Т-лимфоциты перепрограммируются: в них появляется информация об опухолевых клетках, присутствующих в организме пациента.
После перепрограммирования Т-лимфоциты вводят обратно пациенту, она находят раковые клетки и возникает ремиссия. Основные проблемы – создать качественный процесс распознавания и разработать стандартные протоколы лечения.
Много вопросов возникает в понимания биологии заболевания, потому как каждый конкретный случай весьма индивидуален. Мы знакомы только с грубыми поломками, но каждая отдельная поломка провоцирует различное течение болезни.
Мы уже сейчас можем полностью секвенировать геном опухолевой клетки и главное научиться понимать, что в патогенезе является ключевым и как на это можно воздействовать, тогда мы ближе подойдем к полному излечению болезни.
За этим будущее.
Источник: https://leikozu.net/press/stati/kak-postavit-diagnoz-po-analzu-krovi-i-vylechit-oll.html
Пункция костного мозга
Такое исследование проводится под местным обезболиванием и назначается только в том случае, если абсолютное содержание бластных клеток в крови было превышено по анализу, причём настолько, что фактор стресса и инфекционных заболеваний можно сразу же исключить. Тогда у врача появляется основание подозревать лейкоз определенного вида. Чтобы подтвердить или опровергнуть такой диагноз и назначается пункция костного мозга.
Пунктат исследуют под микроскопом, определяется количество бластных клеток. Напомним: в норме оно даже в костном мозге очень мало – около 1%.
Диагноз врача, скорее всего, подтвердится, если по результатам исследования пункции в костном мозге обнаружится более 10% бластов.
Разновидности лейкоза
В медицине существует достаточно много разных форм данного заболевания. В данной статье мы рассмотрим только некоторые, наиболее распространенные. Так, например, имеется острый лейкоз, характеризующийся большим составом молодых бластных клеток. Поэтому можно с точностью сказать, что до 55% всех случаев развивается именно миелобластная форма острого лейкоза.
Так же известен еще острый лимфобластный лейкоз, который чаще всего встречается преимущественно у детей. Кроме этого существует еще некое разделение на подтипы. Так для иммунологического фенотипирования бластных клеток применяют моноклональные антитела. Такие особенности больше важны для правильного исследования и для выявления точного диагноза. Поэтому, формы лейкоза в полной мере учитываются в тонкостях.
Что касается симптомов, то они не всегда совпадают с протеканием заболевания, поэтому довольно сложно выявить на ранней стадии все особенности заболевания.
Интересная информация о бластных клетках (Видео)
Схожие Статьи
Заболевания костного мозга: симптомы, методы диагностики и лечения
Лимфома из клеток мантийной зоны: причины возникновения, симптомы и методы лечения
Миелограмма: что это такое и какие заболевания помогает выявлять?
Что такое лимфома: симптомы, методы лечения и прогноз
Лимфоциты: норма у мужчин, причины и признаки отклонения
Костный мозг: строение, назначение и особенности функционирования
Причина отклонений: лейкоз
Основной причиной появления в пробе бластных клеток является лейкоз. Это заболевание иначе называется лейкемией или раком крови. Патология сопровождается неконтролируемым делением незрелых клеток в костном мозге, которые в дальнейшем образуют опухоль.
Врачи выделяют две формы лейкоза:
- острую;
- хроническую.
При острой лейкемии в крови обнаруживается огромное количество бластных клеток. Их концентрация может быть более 20 %. При хронической форме рака крови показатель незрелых элементов обычно не превышает 5-10 %.
Другие показатели крови
При изучении результатов анализа врач обязательно обращает внимание и на другие показатели клинического исследования. Наличие бластных клеток в биоматериале всегда рассматривается в сочетании с другими параметрами крови. На наличие лейкоза могут указывать следующие данные:
- Лейкоцитоз. Примерно у 15 % больных острой формой лейкемии показатель белых кровяных телец превышает норму в десятки раз.
- Низкий гемоглобин. У пациентов с раком крови отмечается тяжелая анемия и снижение числа эритроцитов.
- Падение уровня тромбоцитов. По этой причине у больных лейкемией отмечается повышенная кровоточивость.
- Снижение ретикулоцитов. Эти клетки являются молодыми формами эритроцитов. Их малое количество приводит к анемии.
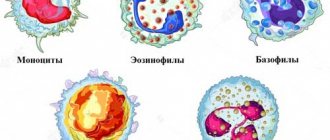
- Полное отсутствие эозинофилов и базофилов. Это становится причиной резкого снижения иммунитета.
Вышеперечисленные признаки вместе с появлением бластных клеток в крови позволяют врачу поставить диагноз «лейкоз».
Что это такое
На преобразование их в зрелые клетки крови потребуется некоторое время. В первую очередь происходит формирование базофильного эритробласта, который имеет ядро в центре. Он отличается круглой формой и размером порядка 18 мкм.
Такие клетки имеют яркий синий цвет. Вскоре из нее происходит образование полихроматофильного эритробласта, который уменьшается в размерах, в сравнении с базофильным. Такие клетки имеют колесный вид хроматина, а цитоплазма становится розово-голубого цвета.
Далее происходит преобразование его в оксифильный эритробласт. Ядро такой клетки, бывшее ранее фиолетового цвета, лишается четкой структуры. Клетка становится еще меньше по размеру и становится уже близка по внешнему виду к такому компоненту крови как эритроциты.
По прошествии некоторого времени ядро становится пикнотичным, а цитоплазма меняет свой цвет на светло-голубой. Это говорит о превращении эритробласта в полихроматофильный. Далее происходит преобразование в ретикулоциты, после чего и образуются в крови зрелые эритроциты, у которых отсутствует ядро.
Подготовка к диагностике
Получив результаты общего анализа, лечащий врач никогда не будет оценивать лишь один его параметр, не обращая внимания на остальные.
Для того чтобы баланс количественного содержания всех форменных элементов крови помимо нормобластов не был искусственно нарушен, следует на протяжении нескольких дней перед диагностикой придерживаться некоторых правил подготовки.
За неделю до процедуры нужно сообщить специалисту перечень принимаемых препаратов, чтобы он мог оценить степень их воздействия на состав крови. Если некоторые медикаменты вызывают нежелательные изменения, их использование временно приостанавливается. За 3–4 дня из рациона изымаются вредные продукты и напитки, особенно фастфуд, алкоголь, маринады, жирная и жареная пища.
Также необходимо на 1–2 дня прекратить спортивные занятия, бег и плавание не являются исключением. Посещать медицинское учреждение следует натощак. Курить перед диагностикой запрещается. Если пациент спешно пришел в клинику, ему обязательно нужно отдышаться, прежде чем заходить в кабинет.
Не рекомендуется накануне забора крови злоупотреблять кондитерскими изделиями – превышение дневной дозировки сладостей влечет за собой ложный результат исследования