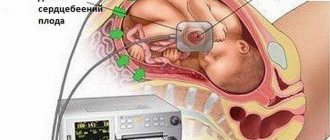
Ультразвуковое исследование плода или перинатальная ультразвуковая диагностика стала совершенно неотъемлемой частью акушерства. УЗИ плода – это огромное подспорье в сложной работе акушеров, однако иногда бывает не совсем понятно, как трактовать некоторые его результаты.
Одним из таких спорных моментов в перинатологии является обнаружение гиперэхогенного фокуса или включения в левом желудочке плода. Такая неожиданная находка, да еще и в сердце неродившегося человека пугает будущую маму. Поговорим о том, что такое гиперэхогенный фокус в сердце плода и опасно ли это.
Описание диагноза
В месте локализации точки обнаруживается уплотнение сердечной ткани, оно может быть вызвано:
- отложениями солей;
- наличием патологии в хромосомном наборе;
- наличием дополнительной хорды, которая не влияет на полноценную работу сердца.
Если причиной, вызвавшей появление белой точки в полости сердца, является большое количество солей, то к третьему триместру она пропадает и не несет никаких последствий для плода. Это же касается и хорды, она может вызывать шумы в сердце до определенного возраста (обычно проходят в 2-3 года), либо исчезает еще до рождения. В любом случае при ее наличии необходимо регулярно обследовать ребенка у кардиолога.
Опасность составляет лишь диагноз, обнаруженный в сочетании с хромосомными нарушениями. В этом случае уплотнение миокарда несет опасность для жизни ребенка.
Гиперэхогенный фокус в левом желудочке сердца плода может свидетельствовать о наличии синдрома Дауна, если при анализе крови у беременной были выявлены патологические хромосомные маркеры.
Возможные осложнения и последствия
Чаще всего добавочная хорда в левом желудочке у крохи пропадает к моменту его рождения, но может присутствовать в сердце до 2-3 -летнего возраста, а может сохраниться на всю жизнь.
Справка! Угрозы благополучию малыша это состояние не несёт, но о нём нужно знать и не игнорировать профилактических визитов к кардиологу.
Участковый педиатр также должен быть предупреждён об особенностях здоровья ребёнка, чтобы исключить ошибочные диагнозы при прослушивании стетоскопом.
На каком сроке сердцебиение плода можно прослушать
Закладка сердца приходится на четвертую неделю беременности. Уже через неделю посредством трансвагинального УЗИ можно обнаружить сокращения миокарда. Ультразвуковое обследование абдоминальным датчиком возможно провести на восьмой неделе. Если на этом сроке отсутствуют сократительные процессы миокарда, то можно делать вывод о замирании беременности.
После формирования сердце сокращается с частотой 110-130 ударов, затем количество значительно увеличивается до 170-190 (пик приходится на восьмую неделю), а после этого удары сердца у плода вновь снижаются до 120-160 за одну минуту и практически не изменяются до родов.
Прослушать сердцебиение посредством использования стетоскопа возможно лишь с двадцатой неделе, доступно это только опытным врачам. Самостоятельно прослушать, как бьется сердце ребенка, можно уже на тридцатой неделе.
Возможности эхокардиографии плода в I триместре беременности (11-14 недель)
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований.
Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Введение
Актуальность темы пренатальной диагностики врожденных пороков сердца (ВПС) понятна всем врачам, которые связаны с пренатальной диагностикой, неонатологией, педиатрией, кардиологией, генетикой. ВПС являются одной из ведущих причин перинатальной смертности и регистрируются с частотой 4-13 на 1000 живорожденных [1]. В связи с тем, что профилактические мероприятия по предупреждению ВПС не имеют должного успеха, представляется актуальной и необходимой их пренатальная ультразвуковая диагностика.
В многочисленных исследованиях зарубежных и отечественных коллег неоднократно формулировались и изучались различные группы риска по возникновению ВПС. Это делалось для того, чтобы потенциально сузить группу беременных женщин, которым показана эхокардиография в специализированном центре. Среди этих групп риска выделяли:
- Семьи, имеющие ребенка с ВПС.
- Семьи с ВПС у одного или обоих супругов.
- Женщин, страдающих сахарным диабетом, системными заболеваниями соединительной ткани, гипотиреозом.
- Беременных с тератогенной экспозицией в ранние сроки беременности (герпес ранее 6-7-й недели) [2].
Однако параллельно другими учеными эти группы риска отвергались, потому что большинство ВПС встречались у плодов и детей, матери которых не входили ни в одну из предложенных групп риска. Единственными разумными критериями так называемого селективного отбора были признаны беременные, попавшие в группу риска после проведения скрининга I триместра и беременные с подозрением на ВПС при ультразвуковом исследовании (УЗИ) плода [3].
Неоспоримо, что оптимальными сроками беременности для исследования сердца плода являются 20-22 недели, однако большинство летальных и клинически значимых пороков сердца могут быть диагностированы в конце I триместра беременности. Позволим себе процитировать слова главы Fetal Medicine Foundation Кипраса Николаидеса, высказанные им на страницах сайта FMF (www.fetalmedicine.com): «Специалист ультразвуковой диагностики с 12 недели беременности должен заверить большинство родителей, что у их ребенка нет крупных врожденных пороков сердца. В случае крупных врожденных пороков сердца их раннее выявление может привести к постановке правильного диагноза или хотя бы вызвать подозрение для осуществления ультразвукового мониторинга».
Главная цель пренатальной диагностики сформулирована специалистами пренатальной диагностики всего мира — это обеспечение женщины максимально возможной информацией о пороке как можно раньше. Мы должны дать право женщине и семье в целом решать вопрос о пролонгировании беременности с грубыми пороками развития у плода [4].
С каждым годом все большее количество публикаций посвящается диагностике ВПС в ранние сроки — в I триместре беременности [5-8]. Практически ни один из выпусков журнала ISUOG (Ultrasound In Obstetrics and Gynecology, или «белого» журнала, как его называют специалисты) не обходит своим вниманием тему ранней диагностики врожденных пороков развития.
На самом знаменитом сайте в мире пренатальной диагностики www.thefetus.net (Philippe Jeanty, USA) опубликовано уже более 30 случаев находок ВПС в I триместре беременности. Однако в отечественной периодике встречаются лишь единичные работы по этой теме. Все они пренадлежат «перу» специалистов пренатальной диагностики Российской ассоциации врачей ультразвуковой диагностики в перинатологии и гинекологии, хотя для многих специалистов как раньше, так и сейчас осмотр сердца плода в сроки 11-14 недель заключается лишь в констатации числа сердечных сокращений.
Цель эхокардиографии в I триместре беременности состоит в выявлении летальных и клинически значимых ВПС. Это исследование не ставит целью выявление стенозов и гипоплазий выносящих трактов, диагностику мелких дефектов перегородок, патологий дуги аорты и артериального протока. Многие из этих пороков не только технически невозможно заподозрить в I триместре, манифестируют они после 30-й недели беременности, т.е. их диагностика является прерогативой исследования III триместра.
Точность пренатальной диагностики ВПС во все сроки беременности варьирует в широком диапазоне. Причинами этого могут быть разный опыт специалистов, ожирение беременной, частота использованных ультразвуковых трансдьюсеров и класс ультразвукового аппарата, перенесенные ранее абдоминальные операции, срок беременности, количество околоплодных вод и положение плода. Однако заметим, что многие из этих факторов теряют свою актуальность именно при проведении трансвагинальной эхокардиографии в I триместре беременности. Своевременная диагностика ВПС позволяет идентифицировать плоды высокого риска по генетическим синдромам, что имеет важное значение при проведении пренатального консультирования и оказывает существенное влияние на акушерскую тактику.
Результаты
С 2006 по 2011 г. пренатально в I триместре беременности были выявлены 125 ВПС. Из них 68 (55%) ВПС сочетались с различными хромосомными аномалиями (ХА) плода, 30 (24%) входили в состав различных множественных врожденных пороков развития (МВПР), 27 (21%) ВПС были изолированными.
При эхокардиографии изучались четырехкамерный срез сердца плода (рис. 1) и срез через три сосуда (рис. 2). УЗИ проводилось трансабдоминальным датчиком, лишь при необходимости (затрудненная визуализация) использовался внутриполостной датчик. Четырехкамерный срез сердца плода при ультразвуковом сканировании трансабдоминальным датчиком визуализировался в 85% случаев, срез через сосуды — в 73%, при использовании трансвагинального датчика эти цифры существенно возрастали до 100 и 91% соответственно. Оптимизация пренатальной диагностики ВПС может быть достигнута путем строгого соблюдения основных методических правил. При оценке четырехкамерного среза плода необходимо оценить нормальное расположение сердца плода, исключив его эктопию (рис. 3), положение оси сердца плода, что не представляет никаких трудностей, нормальные пропорции и размеры камер сердца, движение створок атриовентрикулярных клапанов должно быть свободным, септальная створка трикуспидального клапана должна располагаться ближе к верхушке сердца (рис. 4). При оценке среза через три сосуда необходимо оценить взаиморасположение сосудов и их диаметр.
Рис. 1.
Беременность 12 недель. Четырехкамерный срез сердца плода. Отчетливо видны камеры сердца.
Рис. 2.
Беременность 12 недель. Срез через три сосуда. Визуализируются аорта, легочной ствол. Сосуды расположены в одну линию и имеют нормальные размеры.
Рис. 3.
Беременность 8 недель. Эктопия сердца. Сердце расположено снаружи грудной полости.
Случай опубликован на сайте www.thefetus.net.
Рис. 4.
Беременность 13 недель. Четырехкамерный срез сердца плода. Отчетливо видны камеры сердца. Положение атриовентрикулярных клапанов.
Расширенная эхокардиография предполагает применение дополнительных режимов и срезов — среза через дугу аорты (рис. 5), среза через выносящий тракт левого желудочка (рис. 6), режима ЦДК (рис. 7), импульсной допплерометрии, технологии STIC (рис. 8-11). Это обследование проводится при обнаружении аномальных скрининговых проекций сердца плода, маркеров ХА [расширение толщины воротникового пространства — ТВП, гипоплазия/отсутствие носовой кости (рис. 12, 13), регургитации в венозном протоке (рис. 14), трикуспидальной регургитации (рис. 15)] и/или врожденных пороков развития плода.
Рис. 5.
Беременность 13 недель. Срез через дугу аорты. Отчетливо видны три плечеголовных сосуда, отходящих от дуги.
Рис. 6.
Беременность 12 недель. Тетрада Фалло. Режим ЦДК. Срез через выносящий тракт левого желудочка. Видна «аорта-наездница», сидящая над ДМЖП. Случай опубликован на сайте www.thefetus.net.
Рис. 7.
Беременность 13 недель. Двойной выход сосудов из правого желудочка. Режим ЦДК. Параллельный выход сосудов из правого желудочка.
Рис. 8.
Беременность 12 недель. Атриовентрикулярная коммуникация (АВК) при синдроме Дауна. Режим STIC.
Рис. 9.
Беременность 12 недель. Тетрада Фалло. Режим STIC. Аорта «наездница», сидящая над ДМЖП. Случай опубликован на сайте www.thefetus.net.
Рис. 10.
Беременность 13 недель. Транспозиция магистральных сосудов. Режим STIC. Виден параллельный ход выносящих сосудов, верхний из которых выходит из левого желудочка и делится на бифуркацию (легочная артерия).
Рис. 11.
Беременность 12 недель. Общий артериальный ствол. Режим STIC. Виден единый выносящий сосуд из двух желудочков.
Рис. 12.
Беременность 11,4 недель. Множественные маркеры ХА. Синдром Патау (трисомия 13). Увеличение ТВП, аномальный профиль с гипоплазией носовой кости, протуберансом на верхней челюсти (признак расщелины лица), полидактилия. У плода выявлена гипоплазия левых отделов сердца.
Рис. 13.
Беременность 12 недель. Множественные маркеры ХА. Синдром Дауна (трисомия 21). Увеличение ТВП, аномальный профиль с гипоплазией носовой кости. У плода выявлена АВК.
Рис. 14.
Беременность 12 недель. Реверсный кровоток в венозном протоке у плода с гетеротаксией.
Рис. 15.
Беременность 12 недель. Трикуспидальная регургитация у плода с общим артериальным стволом.
Нозология выявленных нами ВПС была следующей:
- синдром гипоплазии левых отделов сердца (СГЛОС) — 29 случаев (рис. 16);
- атриовентрикулярная коммуникация (АВК) — 23 (рис. 17, 18);
- дефект межжелудочковой перегородки (ДМЖП) — 19 (рис. 19);
- патология магистральных сосудов — 19 (из них транспозиция — 3, двойное отхождение сосудов из правого желудочка — 2, тетрада Фалло — 5, общий артериальный ствол — 9);
- патология правых отделов сердца (патология трикуспидального клапана) — 3;
- синдром гетеротаксии — 6;
- единственный желудочек — 4;
- эктопия сердца — 7;
- сочетанные формы ВПС встретились в 15 случаях.
Рис. 16.
Беременность 13 недель. Синдром гипоплазии левых отделов сердца у плода с синдромом Тернера (45Х). Единый поток через трикуспидальный клапан. Сброс крови в гипоплазированный левый желудочек через ДМЖП.
Рис. 17.
Беременность 11,4 недель. Четырехкамерный срез сердца. Единый атриовентрикулярный клапан. Отсутствует «крест» нормального взаимоотношения атриовентрикулярных клапанов и сердечных перегородок.
Рис. 18.
Беременность 11,4 недель. Четырехкамерный срез сердца. Режим ЦДК. Единый атриовентрикулярный клапан.
Рис. 19.
Беременность 12 недель. Режим ЦДК. Обширный ДМЖП у плода с синдромом Эдвардса (трисомия 18).
При кариотипировании плодов с пренатально установленным диагнозом ВПС в 11-14 недель было диагностировано 68 хромосомных аномалий:
- трисомия 21 (синдром Дауна) выявлена в 23 (34%) случаях,
- трисомия 18 (синдром Эдвардса) — в 19 (28%);
- трисомия 13 (синдром Патау) — в 7 (10%);
- моносомия Х (синдром Тернера) — в 6 (9%);
- триплоидия — в 8 (12%);
- другие хромосомные дисбалансы — в 5 (7%).
Особо следует отметить, что в 8 случаях обнаруженных ХА показанием к кариотипированию было выявление ВПС. У этих плодов было нормальное значение как ТВП, так и длины носовой кости.
При ХА выявленные ВПС по нозологии имели следующие особенности: у большинства плодов с синдромом Дауна диагностировались АВК и ДМЖП; с синдромом Патау — СГЛОС и ДМЖП; с синдромом Эдвардса — ДМЖП, тетрада Фалло и ОАС; при синдроме Тернера — СГЛОС и патология аорты — коарктация аорты в типичном месте (рис. 20).
Рис. 20.
Беременность 12 недель. Срез через дугу аорты. Режим ЦДК. Сужение аорты в «типичном» месте у плода с синдромом Тернера (45Х).
Необходимо отдельно рассмотреть вопрос верификации ультразвукового диагноза. Все беременности с изолированными ВПС в I триместре пролонгировались до срока II триместра, когда возможна 100% морфологическая верификация диагноза. В современных условиях верификация диагнозов после прерывания беременности в I триместре представляет довольно значимую проблему. Однако при специализированном обучении специалистов-морфологов верификация ВПС возможна и при прерывании беременности в I триместре (рис. 21, 22). Это, несомненно, зависит от качества полученного материала, квалификации морфолога и специального оборудования, необходимого в некоторых случаях, а также от общих методологических подходов к анатомо-морфологической диагностике независимо от срока гестации.
Рис. 21.
Беременность 13 недель. Увеличенная ТВП у плода с гипоплазией левых отделов сердца.
Рис. 22.
Тот же плод. Морфологическое обследование — гипоплазия восходящей аорты и кистозные полости (отмечены стрелками).
Заключение
Из сказанного выше можно сделать следующие выводы.
Сердце плода необходимо оценивать у всех беременных при скрининговом осмотре в I триместре (11-14 нед). Так как современная концепция развития пренатальной диагностики в рамках «пилотного» проекта МЗ РФ подразумевает скрининговое обследование в I триместре врачом-экспертом, именно он и должен оценить сердце плода и заподозрить ВПС уже в конце I триместра беременности.
Для исключения летальной и клинически значимой сердечной патологии в I триместре обязательна оценка четырехкамерной проекции сердца плода и среза через три сосуда.
Расширенная эхокардиография должна проводиться при обнаружении аномальных скрининговых проекций сердца плода, маркеров ХА и/или ВПР плода.
При выявлении ВПС в I триместре показано кариотипирование плода.
Литература
- Office for National Statistics. Mortality Statistics. Childhood, Infancy and Perinatal. Series DH3. Stationary Office: London, 2007; 40.
- Новикова И.В., Прибушеня О.В., Румянцева Н.В. Формирование групп риска по дородовой диагностике врожденных пороков сердца. Инструкция по применению. Минск, 2004.
- Carvalho J.S., Moscoso G., Tekay A. et al. Clinical impact of first and early second trimester fetal echocardiography on high risk pregnancies. Heart. 2004; 90: 921-926.
- Becker R., Wegner R.-D. Detailed screening for fetal anomalies and cardiac defects at the 11-13 week scan. Ultrasound Obstet Gynecol 2006; 27; 613-618.
- Allan L.D., Sharland G.K., Milburn A. et al. Prospective diagnosis of 1,006 consecutive cases of congenital heart disease in the fetus. J Am Coll Cardiol 1994; 23: 1452-1458.
- Huggon I.C., Ghi T., Cook A.C. et al. Fetal cardiac abnor-malities identified prior to 14 weeks’ gestation. Ultrasound. Obstet. Gynecol. 2011; 20: 22-29.
- Persico N., Moratalla J., Lombardi C.M. et al. Fetal echocardiography at 11-13 weeks by transabdominal high-frequency ultrasound Ultrasound Obstet. Gynecol. 2011; 37: 296-301
- Allan L.D. Echocardiographic detection of congenitalheart disease in the fetus: present and future. Br. Heart. J. 1995; 74: 103-106.
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований.
Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Диагностика ГЭФа
Обнаружение синдрома «мяча для гольфа» осуществляется при ультразвуковом исследовании. После этого желательно посетить дополнительное 3Д УЗИ, также лечащий врач может направить беременную на эхокардиоскопию плода. Чаще всего данное исследование назначают:
- беременным в возрасте более 35 лет;
- если на раннем сроке у матери были инфекционные заболевания;
- при наличии у беременной (либо родственников) патологий сердца или сахарного диабета;
- после выявления на плановом УЗИ патологий в области сердца;
- при отставании развития плода и его размеров;
- при обнаружении маркеров, свидетельствующих о хромосомных нарушениях.
Гиперэхогенный фокус в левом желудочке сердца плода можно обследовать при помощи эхокардиоскопии на сроке 18-28 недель, после этого провести полноценное обследование не удастся, так как размеры ребенка будут слишком большими, чтобы качественно обследовать размеры и состояние его сердца.
Когда проводят обследование?
Обнаружить гиперэхогенный фокус можно при ультразвуковом исследовании, по итогам которого может быть назначено 3D-УЗИ, либо эхокардиоскопия плода. Поводом к назначению обследования может стать:
- возраст будущей мамы;
- перенесённые в первом триместре беременной женщиной инфекционные болезни;
- сахарный диабет или кардиопатологии у матери или ближайших родственников;
- выявленные ранее проблемы с сердцем у плода;
- отставание ребёнка в развитии (оценивают на УЗИ);
- обнаружение маркеров хромосомных заболеваний.
“Синдром гольфного мяча” хорошо поддаётся определению на эхокардиоскопии, если срок гестации превышает 18 недель, но не достиг 28 недель. Позже полноценно обследовать сердце малыша не удастся, потому что подросший ребёнок частично закрывает обзор.
Показатели нормы при эхокардиоскопии
Во время обследования проводится измерение всех полостей сердца. В норме эти показатели должны находится в пределах:
- длина правого желудочка – 0,5-1,75 см;
- ширина правого желудочка – 0,4-1,1 см;
- длина левого желудочка – 0,9-1,8 см;
- ширина левого желудочка – 0,44-0,89 см;
- отношение показателей ширины левого желудочка к правому – 0,45-0,9 см;
- устье аорты – 0,3-0,52 см;
- устье легочной артерии – 0,3-0,5 см;
- митральное отверстие – 0,35-0,6 см;
- трикуспидальное отверстие – 0,3-0,63 см;
- количество сердечных сокращений – 140-160 ударов/минуту.
Размер сердца плода имеет свои показатели и значительно отличается от размеров взрослого человека, так как все органы соответствуют размерам тела. Патология сердца при таком обследовании выявляется всегда, поэтому не стоит переживать о непрофессионализме узиста, если диагноз не подтвердился или врач говорит, что это не несет угрозы ребенку.
Что необходимо предпринять при выявлении ГЭФа
ГЭФ в сердце плода предполагает назначение врачом дополнительных плановых обследований. К ним можно отнести:
- УЗИ сердца ребенка с допплерографией;
- КТГ (кардиотокография);
- 3Д или 4Д УЗИ.
Если проведенные диагностические методы не опровергли наличие патологий сердца (то есть когда в крови имеются патологические маркеры и на УЗИ эти признаки подтверждаются), рекомендуется посетить генетика.
Такое исследование является очень серьезным шагом, так как несет в себе большую опасность выкидыша или замирание беременности. Поэтому проводить забор пуповинной крови или околоплодных вод необходимо лишь в самых крайних случаях.
Патология сердца может быть незначительной, тогда врач-генетик не будет направлять на такую опасную диагностику. Однако при подтверждении диагноза на объемном УЗИ лучше проконсультироваться с профессионалом на предмет опасности ГЭФ для жизни малыша.
Гиперэхогенный фокус в левом желудочке сердца плода: причины возникновения
Возникновение эхогенного фокуса в сердце ребенка может быть следствием минерализации сосудов сердечной мышцы, индивидуальной особенностью сердца (при которой обнаруживается дополнительная перегородка в сердце в виде небольшой хорды) либо хромосомными патологиями, в частности синдрома Дауна.
Плод по неделям очень быстро развивается и еще больше совершенствуется его тело и жизненно важные системы организма. Именно поэтому нужно регулярно следить за состоянием плода, что позволит вовремя обнаружить возможные проблемы с развитием или предотвратить их до появления первых симптомов.
При наличии патологических хромосомных маркеров в крови матери наличие у ребенка аномалий развития окончательно подтверждается. В этом случае родители должны принимать решение о необходимости дополнительных обследований или прерывания беременности.
Последствия диагноза для ребенка
В норме дополнительная хорда левого желудочка у ребенка исчезает в конце третьего триместра, но она может также находится в сердце всю жизнь, не неся угрозы здоровью. Об этом нужно знать и при необходимости сообщить детском педиатру, так как при прослушивании есть вероятность постановки неправильного диагноза из-за наличия шумов в сердце.
Рекомендуется также стать на учет у детского кардиолога и регулярно обследоваться на предмет наличия патологии. Как правило, к трем годам у ребенка исчезают любые признаки включения в сердечной мышце, тогда врач делает заключение об абсолютном здоровье ребенка.
Стоит ли переживать по поводу данного диагноза
Как правило, гиперэхогенный фокус в левом желудочке сердца плода не несет опасности для ребенка. После рождения и планового осмотра врачом не обнаруживается у детей никаких отклонений от нормы, возможны лишь незначительные шумы при наличии дополнительной хорды.
Когда ребенок достигнет возраста 2-3 месяцев, для большего спокойствия родителей можно сделать УЗИ сердца, в котором подробно будут указаны все размеры полостей и отверстий клапанов, количество дополнительных хорд и общее состояние сердечно-сосудистой системы. В заключении будет написан диагноз о здоровье сердца и полном соответствии возрастным особенностями (обычно до года у деток обнаруживается открытое овальное окно).
Лишь в незначительном проценте случаев дополнительная хорда левого желудочка у ребенка может привести к пороку сердца либо другим патологиям. Но для этого недостаточно одного наличия синдрома «гольфного мяча», необходимо точное подтверждение опасности посредством проведения забора околоплодных вод или крови из пуповины и наличие после диагностики крови патологических маркеров, свидетельствующих о наличии хромосомных аномалий у плода.
Оправданы ли переживания
Несмотря на то что доктора советуют не переживать раньше времени, многие беременные женщины не в силах совладать с эмоциями. Как правило, даже при такой незначительной особенности сердце бьется нормально, не доставляя никакого дискомфорта ребенку.
При наличии гиперэхогенного фокуса левого желудочка сердца плода после рождения ребенка обнаруживаются незначительные шумы в сердце, которые создает особенность структуры миокарда.
По достижении ребенком 2-3-хмесячного возраста назначается ультразвуковая диагностика сердца, после которой выдается заключение с подробным описанием структур сердца, его работы, а также размеров. Редко при такой диагностике может обнаружиться овальное окно — небольшое отверстие между предсердиями. Как правило, такая особенность до года закрывается. Если этого по каким-то причинам не произошло, то назначаются подробные исследования и принимается решение о соответствующем лечении.