Что это такое?
ОМЛ — злокачественная трансформация, охватывающая миелоидный росток кровяных клеток.
Пораженные кровяные тельца постепенно заменяют здоровые, и кровь перестает полноценно выполнять свою работу.
Это заболевание, как и другие типы лейкозов, именуют раком крови в повседневном общении.
Слова, из которых состоит это определение, дают возможность понять его лучше.
Лейкоз. При лейкозе измененный костный мозг начинает активно вырабатывать лейкоциты — кровяные элементы, которые ответственны за поддержание иммунной системы — с патологической, злокачественной структурой.
Они замещают собой здоровые лейкоциты, проникают в разные части организма и формируют там очаги поражения, схожие со злокачественными новообразованиями.
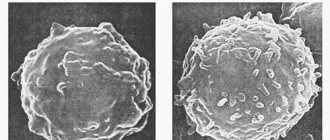
Отличия здоровой крови от больной лейкозом
Миелобластный. При ОМЛ начинается избыточное продуцирование пораженных миелобластов — элементов, которые должны превратиться в одну из разновидностей лейкоцитов.
Они вытесняют здоровые элементы-предшественники, что приводит к дефициту других кровяных клеток: тромбоцитов, эритроцитов и нормальных лейкоцитов.
Острый. Это определение говорит о том, что продуцируются именно незрелые элементы. Если пораженные клетки находятся в зрелом состоянии, лейкоз называется хроническим.
Острый миелобластоз отличается стремительным прогрессированием: миелобласты в крови разносятся по организму и вызывают тканевую инфильтрацию.
Лейкоз
Стадии миелолейкоза и симптомы
Рак крови в своём развитии проходит три стадии:
- Хроническая, при которой больной не испытывает никаких симптомов. Заболевание протекает в скрытой форме. Недомогание и слабость ощущаются заболевшим как симптомы переутомления. С развитием патологического состояния пациент начинает терять в весе, у него пропадает аппетит. В левой части живота, особенно после приёма пищи, появляется боль. Она свидетельствует об увеличении селезёнки. В редких случаях к указанным симптомам может добавляться нарушение зрения, одышка, появляются кровотечения.
- Акселерации, при которой обостряются и нарастают все симптомы хронической стадии. В этой фазе наблюдается упадок сил, обильное потоотделение, беспричинное повышение температуры до 38-39 градусов. Человек постоянно теряет вес, его мучают бесконечные боли в левом подреберье. Увеличенную в размерах селезёнку можно прощупать самостоятельно. На стадии акселерации происходит поражение сердечно-сосудистой системы, которое будет выражаться в частых сердечных приступах, аритмии.
- Терминальная (последняя) стадия миелолейкоза, при которой состояние пациента резко ухудшается. Он ощущает нетерпимые боли в костях, что является результатом поражения злокачественными клетками красного костного мозга. Продолжается потеря веса, держится высокая температура. На теле появляются синяки и кровоподтёки, т.к. снижается количество тромбоцитов. Из-за интенсивного увеличения в размерах селезёнки в животе появляется чувство тяжести, боли и распирания. В это время пациенты очень восприимчивы к различным инфекционным заболеваниям, которые могут стать причиной их смерти.
Симптомы
Обычно ОМЛ развивается у взрослых и пожилых людей. Ранние стадии миелобластной лейкемии характеризуются отсутствием ярко выраженной симптоматики, но, когда заболевание охватило организм, возникают серьезные нарушения многих функций.
Гиперпластический синдром
Развивается из-за тканевой инфильтрации под действием лейкоза. Разрастаются периферические лимфоузлы, увеличивается селезенка, нёбные миндалины, печень.
Поражаются лимфоузлы области средостения: если они разрастаются значительно, то передавливают верхнюю полую вену.
Кровоток в ней нарушается, что сопровождается возникновением отечности в зоне шеи, учащенного дыхания, синюшности кожных покровов, набуханием сосудов на шее.
Также поражаются десна: появляется стоматит Венсана, который характеризуется развитием тяжелых симптомов: десны отекают, кровоточат и сильно болят, есть и ухаживать за полостью рта затруднительно.
Геморрагический синдром
Более половины больных имеют те или иные его проявления, развивается из-за острой нехватки тромбоцитов, при которой стенки сосудов истончаются, нарушается свертывание крови: наблюдаются множественные кровотечения — носовые, внутренние, подкожные, которые долгое время не удается остановить.
Увеличивается риск геморрагического инсульта — кровоизлияния в мозг, при котором летальность составляет 70-80%.
На ранних стадиях острого миелобластного лейкоза нарушение свертываемости проявляется в виде частых носовых кровотечений, кровоточивости десен, синяков на разных частях тела, которые появляются от незначительных воздействий.
Анемия
Характеризуется появлением:
- Выраженной слабости,
- Быстрой утомляемости,
- Ухудшением трудоспособности,
- Раздражительности,
- Апатии,
- Частых болей в голове,
- Головокружений,
- Обмороков,
- Стремления есть мел,
- Сонливости,
- Болей в области сердца,
- Бледности кожи.
Затруднена даже незначительная физическая активность (наблюдается сильная слабость, учащенное дыхание). Волосы при анемии часто выпадают, ногти ломкие.
Интоксикация
Температура тела повышена, вес падает, аппетит пропадает, наблюдается слабость и избыточное потоотделение.
Начальные проявления интоксикации наблюдаются на начальных этапах развития заболевания.
Нейролейкоз
Если инфильтрация затронула мозговые ткани, это ухудшает прогноз.
Наблюдается следующая симптоматика:
- Многократная рвота,
- Острая боль в голове,
- Эпиприступы,
- Обмороки,
- Внутричерепная гипертензия,
- Сбои в восприятии реальности,
- Нарушения слуха, речи и зрения.
Лейкостазы
Развиваются на поздних стадиях заболевания, когда количество пораженных миелобластов в крови становится выше 100000 1/мкл.
Кровь густеет, ток крови становится медленным, нарушается кровообращение во многих органах.
Мозговой лейкостаз характеризуется возникновением внутримозговых кровотечений. Нарушается зрение, возникает сопорозное состояние, кома, возможен летальный исход.
При легочном лейкостазе наблюдается учащенное дыхание (возможно возникновение тахипноэ), озноб, повышение температуры. Количество кислорода в крови сокращается.
При остром миелобластном лейкозе иммунная система крайне уязвима и не способна защищать организм, поэтому высока восприимчивость к инфекциям, которые протекают тяжело и с массой опасных осложнений.
Виды
Миелоидный лейкоз в медицине делят на две разновидности:
- хронический миелолейкоз (наиболее распространённая форма);
- острый миелолейкоз.
Острый миелоидный лейкоз
Острый миелолейкоз
Острый миелоидный лейкоз – заболевание крови, при котором происходит неконтролируемое размножение лейкоцитов. Полноценные клетки заменяются на лейкемические. Патология быстротекущая и без адекватного лечения человек может умереть через несколько месяцев. Продолжительность жизни пациента напрямую зависит от стадии, на которой будет обнаружено наличие патологического процесса. Поэтому важно при наличии первых симптомов миелоидного лейкоза обратиться к квалифицированному специалисту, который проведёт диагностику (наиболее информативным является анализ крови), подтвердит или опровергнет диагноз. Острым миелоидным лейкозом болеют люди из разных возрастных групп, но наиболее часто она поражает лиц старше 40 лет.
Симптоматика острой формы
Симптомы заболевания, как правило, проявляются практически сразу. В очень редких клинических ситуациях состояние больного ухудшается постепенно.
- носовые кровотечения;
- гематомы, которые образуются по всей поверхности тела (один из наиболее важных симптомов для диагностики патологии);
- гиперпластический гингивит;
- ночная потливость;
- оссалгии;
- появляется одышка даже при незначительных физических нагрузках;
- человек часто заболевает инфекционными недугами;
- кожный покров бледный, что свидетельствует о нарушении кроветворения (этот симптом проявляется одним из первых);
- масса тела пациента постепенно снижается;
- на коже локализуются петехиальные высыпания;
- повышение температуры до субфебрильного уровня.
При наличии одного или нескольких таких симптомов рекомендовано как можно скорее посетить медицинское учреждение. Важно помнить, что прогноз заболевания, а также продолжительность жизни пациента, у которого его выявили, во многом зависит именно от своевременно проведённой диагностики и лечения.
Хронический миелоидный лейкоз
Хронический миелоидный лейкоз – это злокачественный недуг, поражающий исключительно гемопоэтические стволовые клетки. Генные мутации происходят в незрелых миелоидных клетках, которые, в свою очередь, продуцируют эритроциты, тромбоциты и практически все виды белых клеток крови. Как следствие, в организме образуется аномальный ген, именуемый BCR-ABL, являющийся чрезвычайно опасным. Он «атакует» здоровые кровяные клетки и преобразует их в лейкозные. Место их локализации – костный мозг. Оттуда с током крови они распространяются по всему организму и поражают жизненно важные органы. Хронический миелолейкоз развивается не стремительно, для него характерно длительное и размеренное течение. Но главная опасность состоит в том, что без должного лечения может перерасти в острый миелоидный лейкоз, который за несколько месяцев способен убить человека.
Болезнь в большинстве клинических ситуаций поражает людей из различных возрастных групп. У детей же возникает эпизодически (случаи заболеваемости очень редки).
Хронический миелоидный лейкоз протекает в несколько стадий:
- хроническая. Лейкоцитоз нарастает постепенно (выявить его можно при помощи анализа крови). Наряду с ним, увеличивается уровень гранулоцитов, тромбоцитов. Также развивается спленомегалия. Вначале недуг может протекать бессимптомно. Позже у пациента появляется быстрая утомляемость, потливость, ощущение тяжести под левым ребром, спровоцированное увеличением селезёнки. Как правило, больной обращается к специалисту только после того, как у него появляется одышка во время незначительных нагрузок, тяжесть в эпигастрии после приёма пищи. Если в данный момент провести рентгенологическое обследование, то на снимке будет отчётливо видно, что купол диафрагмы приподнять кверху, левое лёгкое оттеснено и частично сдавлено, также стиснут и желудок из-за огромных размеров селезёнки. Наиболее страшное осложнение данного состояния – инфаркт селезёнки. Симптомы – боли слева под ребром, иррадиирующие в спину, лихорадка, общая интоксикация организма. В это время селезёнка очень болезненная при пальпации. Вязкость крови повышается, что становится причиной венооклюзивного поражения печени;
- стадия акселерации. На данной стадии хронический миелоидный лейкоз практически не проявляется или же его симптомы выражены в незначительной мере. Состояние пациента стабильно, иногда отмечается повышение температуры тела. Человек быстро устаёт. Уровень лейкоцитов нарастает, также увеличиваются метамиелоциты и миелоциты. Если провести тщательный анализ крови, то в нём обнаружатся бластные клетки и промиелоциты, которых в норме быть не должно. До 30% повышается уровень базофилов. Как только это случается, пациенты начинают жаловаться на появление кожного зуда, чувства жара. Все это обусловлено увеличение количества гистамина. После проведённых дополнительных анализов (результаты которых помещаются в историю болезни для наблюдения тенденции), увеличивается доза хим. препарата, который используют для лечения миелолейкоза;
- терминальная стадия. Эта стадия болезни начинается с появления суставных болей, резкой слабости и повышением температуры до высоких цифр (39–40 градусов). Вес пациента снижается. Характерный симптом для данной стадии – инфаркт селезёнки из-за её чрезмерного увеличения. Человек находится в очень тяжёлом состоянии. У него развивается геморрагический синдром и бластный криз. Более чем у 50% людей на данном этапе диагностируется фиброз костного мозга. Дополнительные симптомы: увеличение периферических лимфоузлов, тромбоцитопения (выявляется по анализу крови), нормохромная анемия, поражается ЦНС (парез, инфильтрация нервов). Продолжительность жизни пациента полностью зависит от поддерживающей медикаментозной терапии.
Причины
Точные причины развития ОМЛ неизвестны, но существует ряд факторов, которые увеличивают вероятность развития заболевания:
- Радиационное облучение. В группе риска люди, которые взаимодействуют с радиоактивными материалами и приборами, ликвидаторы последствий ЧАЭС, пациенты, проходящие лучевую терапию при другом онкологическом заболевании.
- Генетические заболевания. При анемии Факони, синдромах Блума и Дауна риск развития лейкоза увеличивается.
- Воздействие химических веществ. Химиотерапия при лечении злокачественных заболеваний негативно воздействует на костный мозг. Также вероятность повышается при хроническом отравлении ядовитыми веществами (ртуть, свинец, бензол и прочие).
- Наследственность. Люди, близкие родственники которых страдали лейкозами, также могут заболеть.
- Миелодиспластический и миелопролиферативный синдромы. Если лечение одного из этих синдромов будет отсутствовать, заболевание может трансформироваться в лейкоз.
У детей крайне редко фиксируется этот тип лейкоза, в группе риска — люди старше 50-60 лет.
Формы и причины ОМЛ
В зависимости от того, на каком этапе мутировала стволовая клетка, выделяют разные типы миелоидной лейкемии:
- с созреванием или без созревания;
- миеломоноцитарный;
- монобластный (моноцитарный);
- эритробластный;
- мегакариобластный;
- базофильный;
- эозинофильный и другие миелобластные лейкозы.
Также выделяют ОМЛ с минимальной дифференциацией и лейкозы смешанного типа.
В настоящее время существует тенденция определения формы миелоидной лейкемии не по типу клеток, в которые должны были бы развиться бласты, а по видам генетических мутаций в злокачественных клетках. Исходя из данной тенденции, миелобластную лейкемию классифицируют, ориентируясь именно на этот признак.
Важно: не стоит путать острый миелобластный лейкоз с миеломной болезнью. Множественная миелома – лейкоз парапротеинемической формы, который, в свою очередь, входит в группу хронических лимфоцитарных лейкемий.
Причины возникновения ОМЛ у детей и взрослых достоверно неизвестны. Факторами риска являются:
- генетические клеточные мутации, переданные по наследству;
- некоторые хромосомные заболевания;
- врожденный или приобретенный иммунодефицит;
- воздействие радиации, ультрафиолетового излучения, различных канцерогенов, прием определенных лекарственных препаратов – цитостатиков, алкилирующих средств, препаратов, содержащих мышьяк, и некоторых других.
Помимо вышеперечисленных обстоятельств, под вопросом на сегодняшний день находятся теории о взаимосвязи возникновения рака крови миелобластного типа и некоторых вирусных заболеваний, а также вредных привычек.
Считается, что особо высока вероятность заболеть ОМЛ у пациентов, на функционирование организма которых оказывают влияние сразу несколько из упомянутых факторов.
Формы ОМЛ
Миелобластная лейкемия имеет ряд разновидностей, от которых зависит прогноз и тактика лечения.
| Название и классификация по FAB | Описание |
| ОМЛ с незначительной дифференциацией (М0). | Низкая восприимчивость к химиотерапевтическому лечению, легко приобретает резистентность к ней. Прогноз неблагоприятный. |
| ОМЛ без созревания (М1). | Отличается стремительным прогрессированием, бластные клетки содержатся в большом количестве и составляют порядка 90%. |
| ОМЛ с созреванием (М2). | Уровень моноцитов при этой разновидности — менее 20%. Не меньше 10% миелобластных элементов развиваются до стадии промиелоцитов. |
| Промиелоцитарный лейкоз (М3). | В костном мозгу интенсивно накапливаются промиелоциты. Относится к наиболее благоприятным по течению и прогнозу лейкозам — в течение 10-12 лет живут не менее 70%. Симптоматика схожа с остальными разновидностями ОМЛ. Лечится с применением оксида мышьяка и третиноина. Средний возраст заболевших — 30-45 лет. |
| Миеломоноцитарный лейкоз (М4). | Диагностируется у детей чаще, чем другие разновидности заболевания (но в целом ОМЛ в процентном соотношении, по сравнению с другими типами лейкозов, выявляется у детей редко). Лечится с применением интенсивной химиотерапии и пересадки стволовых клеток (ТГК). Прогноз неблагоприятный — показатели выживаемости в течение пяти лет — 30-50%. |
| Монобластный лейкоз (М5). | При этой разновидности в костном мозгу содержится не менее 20-25% бластных элементов. Лечится химиотерапией и ТГК. |
| Эритроидный лейкоз (М6). | Редко встречающаяся разновидность. Лечится с применением химиотерапии и пересадки стволовых клеток. Прогноз неблагоприятный. |
| Мегакариобластный лейкоз (М7). | Этой разновидности ОМЛ подвержены люди с синдромом Дауна. Характеризуется быстрым течением и низкой восприимчивостью к химиотерапии. Детские формы болезни чаще текут благоприятно. |
| Базофильный лейкоз (М8). | Чаще встречается в детском и юношеском возрасте, прогноз жизни М8 неблагоприятный. Помимо злокачественных элементов, в крови выявляются аномальные элементы, которые затруднительно выявить без специального оборудования. |
Также, помимо упомянутых разновидностей, существуют и другие редкие виды, не внесенные в общую классификацию.
Причины и механизмы развития
Острый миелоидный лейкоз (ОМЛ), как любые лейкозы, возникает из одной мутировавшей клетки, которая теряет способность созревать и начинает бесконтрольно размножаться. Сказать точно, какие именно из известных канцерогенных факторов спровоцировали мутации в каждом конкретном случае обычно невозможно, особенно если речь идет о детях. В целом это могут быть:
- Биологические факторы: онкогенные вирусы, самый известный из которых – Эпштейн-Бара.
- Химические вещества. Всего известно более полутора тысяч канцерогенных соединений. К ним относятся: продукты неполного сгорания табака; вещества, возникающие при неполном окислении жиров (жарение во фритюре); производственные «вредности», появляющиеся при термической обработки нефти, смол, угля; продукты жизнедеятельности плесеней; лекарства, применяемые для химиотерапии злокачественных опухолей (как ни печально, известны случаи, когда лейкоз возникает через 10-20 лет после успешного избавления от рака).
- Физические факторы. В основном это ионизирующее или рентгеновское излучение: известно, что для работников ренгтгенкабинетов вероятность заболеть выше, чем в среднем по популяции.
Кроме внешних воздействий имеет значение наследственность: известен, например «лейкоз близнецов», или передающийся в семье из поколения в поколение. Наследуется не сама болезнь, но генные или хромосомные мутации, повышающие ее вероятность. Помимо этого, некоторые врожденные патологии сочетаются с большей частотой развития лейкозов, в частности, миелолейкоза:
- синдром Дауна;
- нейрофиброматоз 2 типа;
- анемия Фалькони;
- тяжелая врожденная анемия;
- врожденная тромбоцитопения или тромбоцитопатия.
В основе патогенеза, или механизма развития, миелобластного лейкоза – конкуренция между нормальными и опухолевыми клетками. Первоначально одна-единственная атипичная клетка за 3 месяца она способна породить 1012 – один триллион – дочерних бластов, общей массой более килограмма. Злокачественные клетки дольше живут, так как у них отключается механизм «старения» и естественной гибели. Они вырабатывают вещества, угнетающие активность здоровых элементов крови, подавляющие ростовые факторы. В такой ситуации возможности нормального кроветворения постепенно истощаются.
Кроме того, организм, «видя» огромное количество миелобластов в костном мозге, сосудистом русле, начинает замедлять активность кроветворения: поскольку все клетки так или иначе дифференцируются из бластных, он воспринимает дегенеративные, злокачественный клетки как «нормальные». Это еще один механизм, позволяющей онкологии выиграть конкуренцию. По мере развития гемобластоза, злокачественные клетки начинают размножаться в других тканях и органах: печени, селезенке, лимфоузлах, коже и даже мозговых оболочках.
Именно замена здоровых клеток крови на массу бластов, неспособных выполнять их функции в силу незрелости, формирует симптомы белокровия.
Диагностика
Острая лейкемия выявляется с применением ряда диагностических мероприятий.
Диагностика включает в себя:
- Развернутый анализ крови. С его помощью выявляется содержание в крови бластных элементов и уровень остальных кровяных телец. При лейкемии обнаруживается избыточное количество бластов и сниженное содержание тромбоцитов, зрелых лейкоцитов, эритроцитов.
- Взятие биоматериала из костного мозга. Применяется для подтверждения диагноза и проводится после проведенных обследований крови. Этот метод применяется не только в процессе диагностики, но и на протяжении лечения.
- Биохимический анализ. Дает информацию о состоянии органов и тканей, содержании различных ферментов. Этот анализ назначается для получения развернутой картины поражения.
- Другие виды диагностики: цитохимическое исследование, генетическое, УЗИ селезенки, брюшной полости и печени, рентген зоны груди, диагностические мероприятия для выявления степени поражения головного мозга.
Могут быть назначены и другие методы диагностики, в зависимости от состояния пациента.
Диагностика и анализы при миелоидном лейкозе
При подозрении на миелоидный лейкоз пациенту предлагается пройти ряд исследований — УЗИ диагностику органов брюшной полости и лабораторные анализы крови:
- Общий анализ крови.
- Биопсия красного костного мозга.
- ПЦР крови.
- Цитогенетическое исследование крови.
УЗИ органов брюшной полости
На хронической стадии болезни происходит увеличение селезёнки в размерах. На этапе акселерации УЗИ селезёнки и печени показывает их увеличение более чем на 10 см, а во время бластного криза селезёнка достигает огромных размеров — она занимает почти всю брюшную полость. Её вес колеблется в пределах 5-8 кг.
Подготовка к ультразвуковому исследованию органов брюшной полости проводится натощак. Пить воду тоже нельзя как минимум за 4 часа до процедуры. За 2 дня до этого из меню исключаются все продукты, способные привести к газообразованию, а также алкогольные напитки. Пациентам, страдающим запорами, рекомендуют провести очистительную клизму. Перед УЗИ нельзя курить.
Результаты исследования пациент получает сразу после процедуры.
Общий анализ крови
Когда больной приходит к врачу с жалобами на общее недомогание, головные боли и усталость, врач отправляет его на общий анализ крови, который является очень результативным и показательным при многих заболеваниях. Несмотря на то что они имеет множество показателей, поставить диагноз всего лишь на этом исследовании невозможно.
Сдаётся анализ утром, натощак. Необходимо исключить за сутки употребление в пищу жирных продуктов, т.к. это может исказить результат. В качестве биологического материала используют капиллярную кровь из подушечки пальца. Обычно результат бывает готов через несколько часов.
На хроническом этапе распознать заболевание сможет только общий анализ крови, который показывает при наличии патологического процесса увеличение незрелых клеток крови, базофилов (больше 0,1%), эозинофилов (более 5%) и серьёзное увеличение лейкоцитов (более 9 тысяч) и понижение тромбоцитов без особых причин (у взрослого — менее 180, у детей с года — менее 160).
На стадии акселерации общий анализ крови показывает:
- число миелобластов увеличивается до 20% — у здорового человека их быть в крови не должно;
- количество базофилов увеличивается до 20%
- до 100 тысяч единиц снижается уровень тромбоцитов;
- продолжает расти число лейкоцитов.
На терминальной стадии общий анализ крови свидетельствует:
- об увеличении числа миело и лимфобластов на 20 и более процентов;
- о появлении в костном мозге больших скоплений бластов.
Это незрелые клетки крови, которые в дальнейшем преобразуются в кровяные тельца. При отсутствии патологии в крови они не встречаются. Поэтому при обнаружении бластов в крови проверяют и костный мозг на их наличие.
Исследование красного костного мозга при миелобластном лейкозе
Клетки крови вырабатываются красным костным мозгом. Для того чтобы подтвердить диагноз, проводят пункцию красного костного мозга и отправляют на исследование часть кости. Чаще всего биопсию берут из грудинных, тазовых (у взрослых), пяточных костей (у детей до 2-х лет).
Врач под местной анестезией специальным шприцем с иглой прокалывает кость — у взрослых на глубине 3-4 см, у детей — 1-2 см — и набирает в шприц ткань из полости кости. Затем полученный биоматериал наносят на стёкла и изучают под микроскопом в лаборатории.
Подготовка к процедуре будет заключаться в следующем: проводится беседа с врачом о наличии аллергической реакции на анестетик. Кроме того, пациенту, принимающему кроверазжижающие препараты, рекомендуют воздержаться от них в течение 2-х недель.
Накануне пункции больному нужно очистить кишечник и мочевой пузырь, принять душ, мужчине удалить растительность на груди в месте прокола. Больному даётся успокоительное, за 30 минут анестетик. После этого доктор прокалывает мягкие ткани в районе кости, нащупывает её и вводит туда иглу со шприцем, осуществляя забор биоматериала. После этого место прокола обрабатывается антисептиком. Время процедуры — 20-30 минут. Исследование образца занимает от 2 до 4 часов, в некоторых случаях — при отсутствии собственной лаборатории — на получение результата может уйти до месяца.
Пациент может через 30 минут отправиться домой. В течение 3 дней нельзя принимать душ и ванну, чтобы не мочить место прокола.
Пункция красного мозга не проводится в следующих случаях:
- при остром инфаркте миокарда;
- при остром нарушении мозгового кровообращения;
- при гипертоническом кризе;
- во время приступа стенокардии.
На хронический миелолейкоз в результатах анализа указывает количество лейкоцитов, выше 17 у взрослых и более 35% у детей после 5 лет. Если количество бластов (эритробласты, нормобласты) повышено на 20% — речь идёт об остром лейкозе.
ПЦР на наличие гена BCR — ABL1
Метод полимеразно-цепной реакции позволяет с высокой точностью определить не только наличие вирусов, но и хромосомные аномалии. ПЦР направлен на поиски гена BCR — ABL1, вызывающего рак крови. Это очень сложный химический процесс, требующий специальных лабораторных условий и высокой квалификации профессионалов.
Для анализа берут венозную кровь или красный костный мозг. Если требуется анализ крови, то у больного утром натощак берётся венозная кровь. Для достоверности анализа рекомендуется не применять лекарственных препаратов за 2 недели до анализа. Результаты готовятся в течение суток. Если обнаружен ген BCR — ABL1, даже в небольших количествах, значит диагноз хронического миелолейкоза подтверждается.
Цитогенетическое исследование на наличие Ph филадельфийской хромосомы
Наличие филадельфийской хромосомы подтверждает диагноз миелобластный лейкоз. Эта хромосома появляется в результате объединения двух участков на 22-ой хромосоме. Поиск Ph проводится методом ПЦР, о котором говорилось выше.
Данная хромосомная аномалия наблюдается в 95% случаев хронической стадии болезни, значит этот метод помогает определить заболевание на ранней стадии.
Лечение
Лечение ОМЛ включает применение следующих методов:
- Химиотерапия. Медикаменты воздействуют на клетки, подавляя их активность и размножение. Ключевой метод лечения лейкемии.
- Консолидация. Лечение, назначаемое во время ремиссии, нацелено на снижение вероятности рецидива.
- Трансплантация стволовых клеток. Пересадка костного мозга при лейкозе применяется при лечении больных младше 25-30-летнего возраста и необходима в тех ситуациях, когда заболевание течет неблагоприятно (наблюдается нейролейкоз, концентрация лейкоцитов крайне высока). Пересаживаются либо собственные клетки, либо донора. Обычно донорами становятся близкие родственники.
- Дополнительная терапия. Восстанавливает состояние крови, включает введение кровяных элементов.
Также может быть применена иммунотерапия — направление, использующее иммунологические препараты.
Применяются:
- Медикаменты на основе моноклональных антител,
- Адаптивная клеточная терапия,
- Ингибиторы контрольных точек.
При таком диагнозе, как острый миелолейкоз, продолжительность лечения составляет 6-8 месяцев, но может быть увеличена.
Клиническая картина
Проявления острого миелолейкоза неспецифичны – это значит, что на начальном этапе симптомы напоминают признаки других заболеваний.
Анемический синдром
Из-за недостаточности кроветворения уменьшается количество эритроцитов. Общая слабость, бледность, ломкость ногтей и выпадение волос обычно либо не привлекают внимания пациента или его родственников, либо связываются с другими проблемами. По мере развития болезни слабость нарастает появляется одышка даже при минимальных нагрузках, дети перестают играть в подвижные игры (вообще, снижение активности ребенка – повод внимательно присмотреться к его здоровью).
Геморрагический синдром
В крови становится мало не только эритроцитов, но и тромбоцитов. Нарушается свертываемость крови. Возникают кровотечения различной интенсивности: от точечных подкожных кровоизлияний до обильных внутриполостных (желудочно-кишечных, маточных и т.д.).
Инфекционный и интоксикационный синдромы
Гранулоцитарные лейкоциты, принадлежащие к миелодиному ростку – это клетки, чья функция – защищать организм от микробов. Они содержат множество белков – естественных антибиотиков, перекисей, других веществ, направленных на уничтожение инфекционного агента. Угнетение кроветворного ростка затрагивает и их, нарушая способность организма бороться с болезнетворными микробами. Это проявляется различными гнойными воспалениями: кожными абсцессами, флегмонами, вплоть до сепсиса. Любое воспаление вызывает интоксикацию – отравление продуктами обмена веществ патогенных микроорганизмов. Интоксикационный синдром проявляется такими признаками как:
- слабость;
- повышение температуры;
- потливость;
- потеря аппетита, снижение веса;
- неопределенные боли в мышцах.
Гиперпластический синдром
Отмечается у 30-50% пациентов. Опухолевые клетки заполняют не только костный мозг, но и лимфоузлы, печень, селезенку. Органы увеличиваются, оставаясь безболезненными, их консистенция становится тестообразной. Сама по себе гиперплазия не опасна, но если разрастаются лимфоузлы, которые находятся в замкнутом пространстве (например, полости средостения, где расположено сердце) они могут сдавить жизненно важные органы.
Нейролейкоз
У 5-10% детей лейкозные клетки создают «метастазы» — участки размножения опухолей в полости черепа, мозговых оболочках, крупных нервах. В результате возникают признаки поражения этих органов: нарушение чувствительности и функции конечностей при инфильтрации периферических нервов, симптомы менингита и опухоли мозга при разрастании инфильтрата внутри полости черепа.
Лейкозные клетки могут образовывать участки экстрамедуллярных (в дословном переводе – расположенных вне костного мозга) опухолей в костях, на коже и слизистых, молочных железах, матке и придатках, простате, легких. При этом возникают симптомы, характерные для патологии этих органов.
Прогноз жизни
Прогноз зависит от следующих факторов:
- Типа ОМЛ,
- Чувствительности к химиотерапии,
- Возраста, пола и состояния здоровья пациента,
- Уровня лейкоцитов,
- Степени вовлеченности головного мозга в патологический процесс,
- Продолжительности ремиссии,
- Показателей генетического анализа.
Если заболевание чувствительно к химиотерапии, концентрация лейкоцитов умеренная, а нейролейкоз не развился, прогноз положительный.
При благоприятном прогнозе и отсутствии осложнений выживание в течение 5 лет составляет более 70%, частота рецидивов менее 35%. Если состояние пациента осложнено, то выживаемость равняется 15%, при этом рецидивировать состояние может в 78% случаев.
Чтобы своевременно выявить ОМЛ, необходимо регулярно проходить плановые медицинские обследования и прислушиваться к организму: частые кровотечения, быстрая утомляемость, возникновение синяков от небольшого воздействия, длительное беспричинное повышение температуры могут говорить о развитии лейкоза.
Лечение острого миелолейкоза
Состоит из сопроводительной терапии (СТ) и противоопухолевой химиотерапии (ПХТ). СТ универсальна для всех видов острого лейкоза. Отсутствие адекватной СТ исключает достижение эффекта от ПХТ. Различают индукционную и консолидирующую ПХТ, которая должна проводиться в специализированных лечебных учреждениях. Индукционная терапия должна включать антрациклины и цитозинарабинозид. Пациенты, не ответившие на один-два цикла, признаются рефрактерными. При достижении клинико-гематологической ремиссии проводятся от одного до нескольких курсов консолидирующей терапии цитозинарабинозидом. Больным с промежуточным или плохим прогнозом при отсутствии родственного донора показана неродственная аллогенная трансплантация. Исходами терапии острого лейкоза могут быть: ремиссия заболевания (длительностью более 5 лет — выздоровление), ранняя летальность (смерть в период первого, второго курса химиотерапии) или первичная резистентность (отсутствие ремиссии после двух курсов химиотерапии).
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.
- Даунорубицин (антрациклиновый противоопухолевый антибиотик). Режим дозирования: в/в, дозу препарата подбирают индивидуально, с учетом состояния пациента и применяемой схемы лечения.
- Цитарабин (противоопухолевое, иммунодепрессивное средство). Режим дозирования: в/в, в дозе 100 мг/м2/сут., две капельные инфузии по 3 ч каждая с интервалом 10 ч или непрерывно в течение 24 ч, на курс — 500–1000 мг. П/к, в дозе 20 мг/м2 2–3 раза в сутки. Курс — 4–7 дней (максимально до 10 дней).
Пересадка костного мозга
Данная процедура значительно увеличивает вероятность выздоровления пациента. В качестве донора часто выступают родственники больного. После проведения различных тестов на совместимость, пациента начинают готовить к операции около одной недели. За этот период времени он проходит курс лучевой и химиотерапии.
При операции в кровоток пациента поступают донорские стволовые клетки, которые накапливаются в костном мозге и уже через один месяц начинают там функционировать. В этот период времени у больного снижен иммунитет, поэтому ему назначают медикаментозные препараты для снижения риска отторжения донорских клеток. Также врач назначает антибактериальные и противогрибковые медикаменты. Постепенно самочувствие больного улучшается, кости и мягкие ткани, кровь очищаются от патологических клеток и начинают нормально функционировать. Полное восстановление проходит через несколько месяцев, в этот временной срок пациент находится под наблюдением лечащего врача.
Обратите внимание! Полное выздоровление возможно только при пересадке стволовых клеток. В этом случае они должны полностью одинаковыми у пациента и у донора.
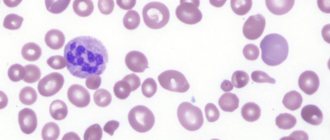
Что такое хронический миелолейкоз?
Мазок крови пациента с хроническим миелолейкозом
Хронический миелолейкоз (ХМЛ) — злокачественное новообразование кроветворной ткани, сопровождающееся прогрессирующей пролиферацией незрелых гранулоцитов. Заболевание изначально обладает вялотекущим характером, постепенно перетекая в стадию обострения с выраженной симптоматикой и образованием системных нарушений. Является одной из самых опасных и инвалидизирующих болезней.
ХМЛ — первое онкологическое заболевание, у которого определена связь между развитием канцерогенеза и мутацией в гене. Характерная аномалия основана на транслокации 9-й и 22-й хромосом, то есть участки данных хромосом меняются местами, образуя аберрантную хромосому. Выявлена мутировавшая хромосома исследователями из Филадельфии, поэтому она получила название филадельфийская или Ph-хромосома.
Изучение Ph-хромосомы и её влияния позволило разработать новое средство для подавления онкологических процессов, благодаря которому продолжительность жизни пациентов значительно увеличилась. Однако болезнь до сих пор остаётся неизлечимой. Число первичных ХМЛ диагностируется у 1,5:100 000 населения в год, пик заболеваемости приходится на возраст 30-50 лет, 30% ХМЛ выявляется у лиц старше 60 лет, у детей заболевание диагностируется менее чем в 5% случаев.
В чем суть проблемы?
На картинке можно увидеть, какой состав крови у здорового человека, и как она меняется при лейкозе:
Многих, естественно, волнует вопрос: что это такое? Острый миелолейкоз (или резко миелоцитарный лейкоз) – это патология онкологического характера, затрагивающая систему крови, когда отмечается неконтролируемое размножение лейкоцитов измененной формы. Кроме того, в анализе крови будут присутствовать и такие проблемы, как уменьшение количества эритроцитов, тромбоцитов и лейкоцитов из категории нормальных.
Заболевания крови отличаются особой опасностью для человека. И это неспроста, ведь именно кровь находится в тесном контакте со всеми органами и системами в организме, именно она является переносчиком жизненно важного гемоглобина и кислорода. Поэтому крайне важно, чтобы кровообращение было налажено полностью и правильно. Клеточный же состав должен оставаться в пределах нормы.
Под острым миелобластным лейкозом (ОМЛ) понимают состояние, когда изменяются незрелые клетки крови, названные бластами. В это же время в организме ощущается недостаток зрелых клеток. Измененные бласты увеличиваются фактически в геометрической прогрессии.
Тут важно понимать, что процесс изменения клеток необратим и не контролируется никакими лекарственными препаратами. Лейкемия бластных клеток – тяжелое и угрожающее жизни заболевание.
Обычно все патпроцессы в такой ситуации локализуются в костном мозге и периферической системе кровообращения. Злокачественные клетки активно подавляют не сломанные и не испорченные и начинают заражать буквально все в теле.
Что такое лейкоз и можно ли его предотвратить? Что такое химиотерапия? Ответы на вопросы узнаете, посмотрев следующее видео:
Стадии развития заболевания
Миелоидная лейкемияхронического характера имеет три стадии развития:
- Хроническая стадия развивается при отсутствии своевременного лечения, заболевание на данном этапе диагностируется у 85% пациентов. В этот период наблюдается стабильность в состоянии больного, признаки патологии проявляются в минимальном количестве и не причиняют дискомфорта. Продолжительность этой стадии составляет от трех до четырех лет в зависимости от того, насколько рано было начато лечение. Обычно ХМЛ выявляется случайно при проведении анализа крови. Если лечение не было вовремя начато, наступает следующая стадия заболевания.
- Акселеративная стадия, при которой начинается активный рост аномальных клеток крови. Данная фаза протекает около одного года, при этом возможно развитие новых патологий в дополнение к аномальной хромосоме.
Обратите внимание! Число незрелых лейкоцитов на этой стадии постоянно растет, но существует возможность вернуть заболевание в хроническую фазу при использовании правильного лечения. В противном случае развивается последняя стадия недуга.
- Бластный криз или терминальная стадия, что является последней фазой заболевания, характеризуется наличием новых аномалий хромосом. Здесь костный мозг полностью замещается патологическими клетками. Эта фаза болезни имеет схожесть с острым лейкозом, прогнозпри неэффективном лечении неблагоприятный, недуг заканчивается летальным исходом. Обычно длится бластный криз около шести месяцев.
Некоторые больные при постановке диагноза уже находятся на терминальной стадии развития патологии, поэтому риск развития смертельного исхода в этом случае очень высок.
Причины развития проблемы
Белокровие, острый миелоидный лейкоз – все это одно и то же название такой патологии. Естественно, что многих волнует, что приводит к развитию такой проблемы. Но, как и в случае с другими видами онкологии, врачи со 100% уверенностью не могут назвать катализатор изменения клеток крови. Однако возможность выделить предрасполагающие факторы есть.
На сегодняшний день основной причинойразвития патологии называют хромосомные нарушения. Обычно имеют в виду ту ситуацию, которая названа «филадельфийская хромосома». Это состояние, когда из-за нарушения начинают меняться местами целые участки хромосом, образуя совершенно новую структуру молекулы ДНК. Дальше быстро образуются копии таких злокачественных клеток, что и приводит к распространению патологии.
К такой ситуации, по мнению медиков, могут приводить:
- Облучение радиацией. Так, например, в зоне риска те, кто находится на производственных участках с большим количеством излучения, спасатели, работающие на месте разбора завалов, как это было на Чернобыльской АЭС, пациенты, проходившие ранее облучение для терапии иного вида онкологии.
- Некоторые вирусные заболевания.
- Электромагнитные излучения.
- Воздействие ряда лекарственных средств. Обычно в этом случае имеют в виду терапию против рака из-за ее повышенной токсичности на организм.
- Наследственность.
Те, кто в группе риска, обязательно должны регулярно проходить обследование.
Патогенез
Заболевание развивается вследствие случайной хромосомной аномалии, происходящей в стволовой клетке. В норме стволовые клетки могут развиваться в разные виды клеток организма, среди них и те, которые являются элементами крови. Но при перегруппировке двух хромосом (9 и 22) в так называемую филадельфийскую хромосому образуется тирозинкиназа – аномальный фермент. Он приводит к повышенной продукции лейкоцитов, постепенно размножающихся и заполняющих костный мозг. Далее клетки попадают в периферическую кровь, селезенку и печень. В некоторых случаях развиваются дополнительные мутации, приводящие к устойчивости миелолейкоза к лечению.
При развитии хронического миелоидного лейкоза основная часть лейкоцитов продуцируется в костном мозге. Но некоторые из них также вырабатываются в печени и селезенке.
Если при остром лейкозе в организме есть много бластных клеток, то при хронической форме существенно увеличивается количество лейкоцитов, кажущихся нормальными, а в некоторых случаях – и тромбоцитов.
Постепенно происходит изменение лейкозных клеток, и болезнь переходит в фазу акселерации, после которой наступает фаза бластного криза, когда продуцируются только незрелые лейкозные клетки. Соответственно, состояние усугубляется, и у больного часто увеличивается селезенка, повышается температура, теряется вес.
Прогноз и профилактика
При диагностировании хронической стадии заболевания и своевременно проведенной пересадке костного мозга возможно полное выздоровление пациента. Большая часть людей умирает при наличии у них фазы акселерации или бластного криза. У 10% из них смертельный исход происходит в течение двух лет после постановки диагноза. При терминальной стадии развития заболевания человек может прожить еще полгода, если же лечение дало положительные результаты, началась ремиссия, то продолжительность жизни увеличивается до одного года.
Методов профилактики ХМЛ в современной медицине не разработано, так как до сих пор не выяснены точные причины развития патологии. Медики рекомендуют вести здоровый образ жизни, не злоупотреблять медикаментозными препаратами при лечении различных заболеваний, а также избегать воздействия радиации.
(2 оценок, среднее: 5,00 из 5)
Лечение онкологии крови
На начальной стадии развития заболевание лечение используют медикаментозное. Медики часто назначают «А-интерферон», «Миелосан». Облегчение наступает на шестой неделе приема препаратов. Потом проводится поддерживающая терапия, в случае обострения заболевания проводят курсы лечения «Миелосаном». Если данный препарат оказывается неэффективным, используют «Миелобромол» на протяжении трех недель. В крайнем случае, врач назначает «Допан» или «Гексафосфамид».
Также для лечения патологии прибегают химиотерапии с использованием химических препаратов, которые снижают рост опухолевых клеток, способствуют их разрушению. Данный метод используют на разных стадиях недуга. Он имеет побочные действия, что выражаются в нарушении деятельности ЖКТ, появлении аллергических реакций, болей в мышцах, судорогах. После курса химиотерапии врач назначает «Интерферон» с целью восстановления иммунной системы.
Если химиотерапия оказалась неэффективной, прибегают к лучевой терапии. Также ее могут использовать при подготовке пациента к пересадке костного мозга.
Обратите внимание! В некоторых случаях проводят удаление селезенки из-за наличия сильного болевого синдрома в области живота, значительного увеличения органа или при угрозе его разрыва.
С целью предотвращения развития микроскопических тромбозов и отека сетчатки глаз медики назначают лейкоцитофорез. В данном случае проводится очистка крови от патологических клеток.